Chemia dnia codziennego – podsumowanie
Wszystko, co nas otacza, jest zbudowane z substancji chemicznych. Każda substancja charakteryzuje się określonym składem, budową i właściwościami. Różnorodność występujących w przyrodzie minerałów stwarza duże możliwości ich wykorzystania w praktyce.

1. Ditlenek krzemu - w stanie wolnym i w postaci związanej
Krzemionka – tlenek krzemu(IV) – to podstawowy składnik piasku, skał i gleb. Już od najdawniejszych czasów ludzie wykorzystywali niezwykłe właściwości tej substancji.


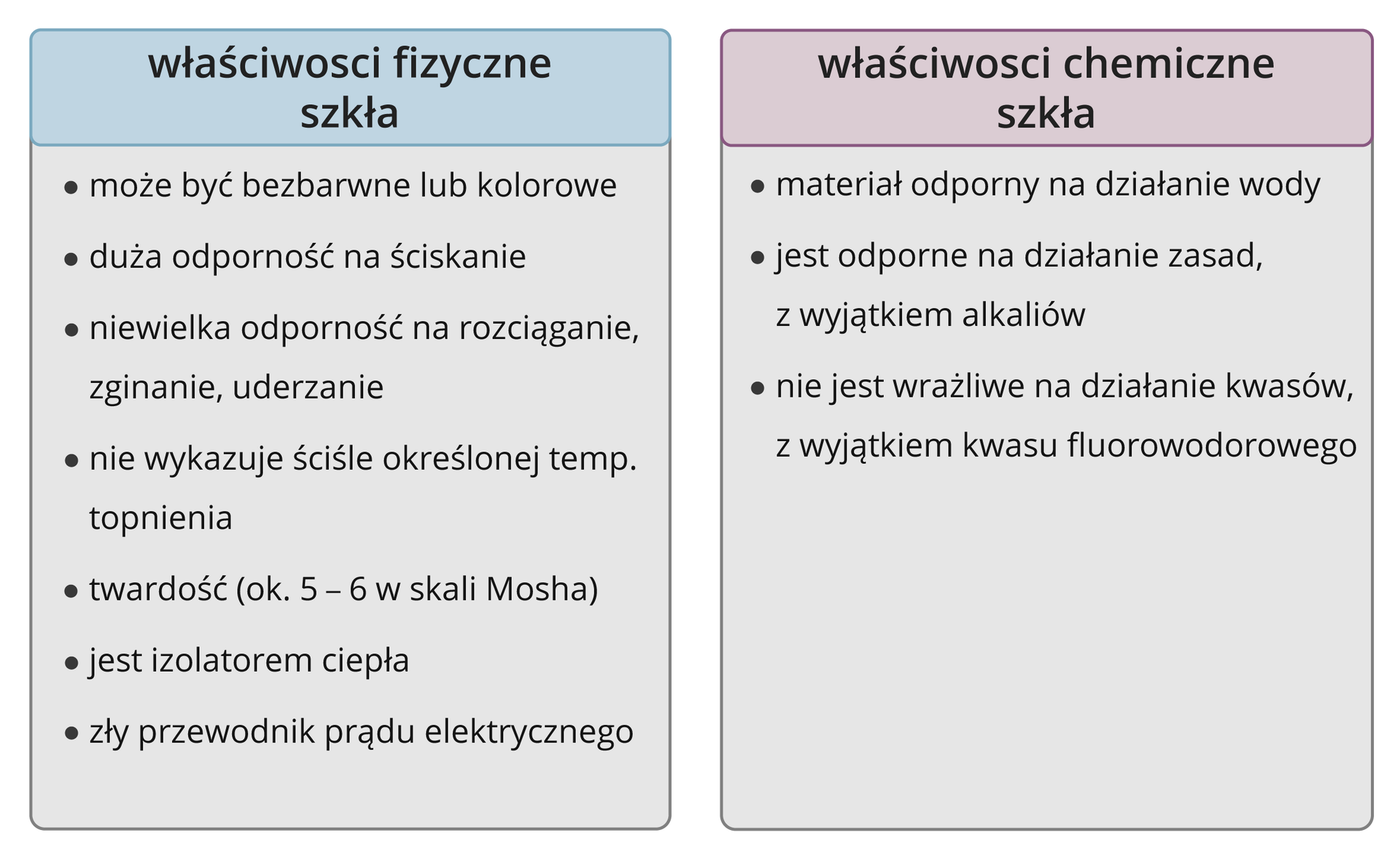
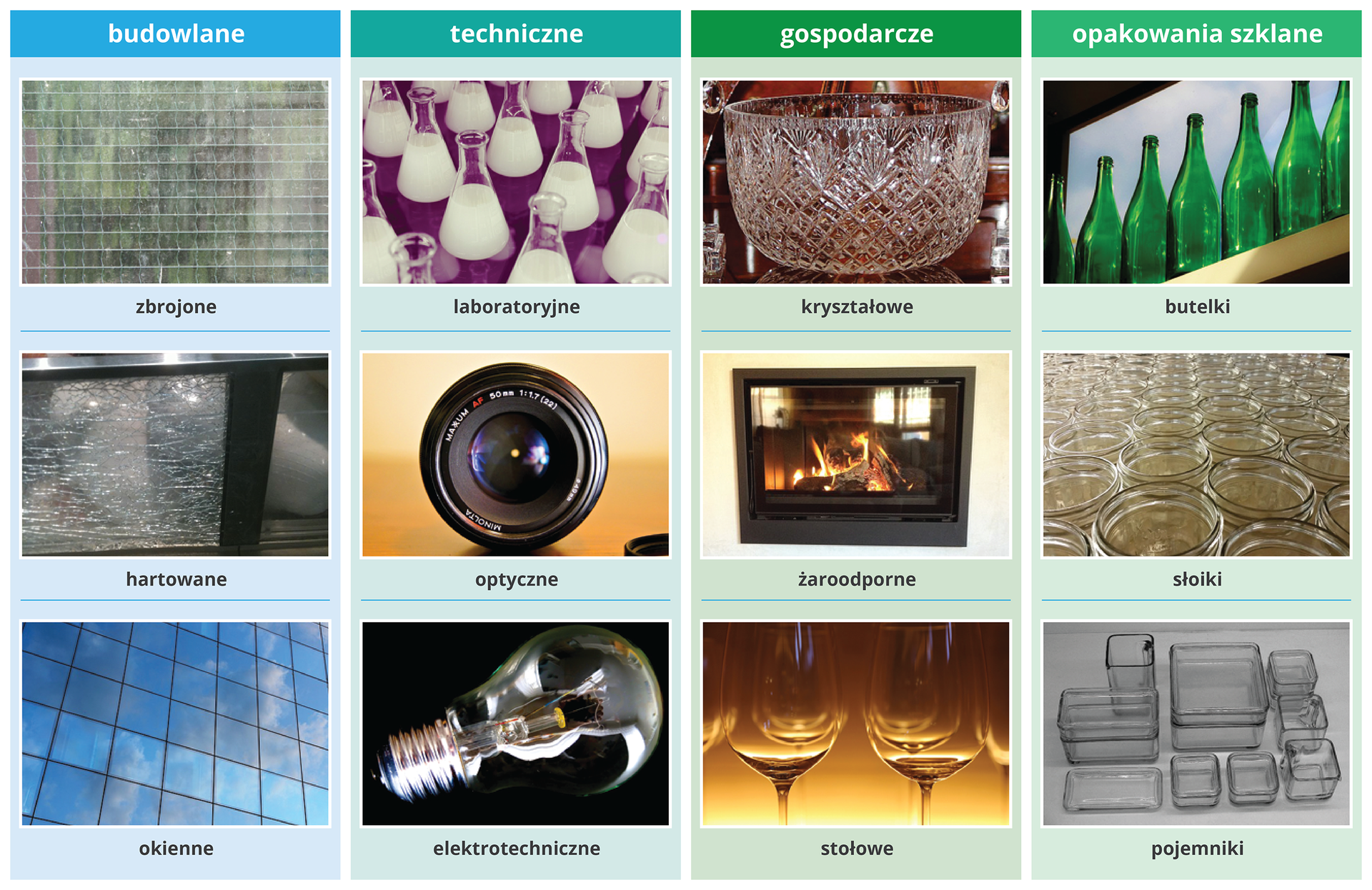
2. Szkło
Szkło jest materiałem bezpostaciowym, który otrzymuje się w wyniku stopienia mieszaniny piasku kwarcowego (), wapienia () i sody () oraz stłuczki szklanej. Każdy rodzaj szkła ma określone właściwości i wynikające z nich zastosowanie.
3. Skały wapienne i skały gipsowe
W skład minerałów i skał, które budują skorupę ziemską, wchodzi wapń. Pierwiastek ten jest głównym składnikiem skał wapiennych oraz skał gipsowych. Rola chemików w pozyskiwaniu i przemysłowym przetwarzaniu zasobów Ziemi jest nieoceniona.
Skały wapienne | Skały gipsowe |
Skała RękawicaSkała Rękawica w Ojcowskim Parku Narodowym jest zbudowana z jurajskich wapieni. | Jaskinia SkorocickaJaskinia Skorocicka w Górach Świętokrzyskich to najdłuższa jaskinia gipsowa w Polsce. |
Skały wapienne to skały, których głównym składnikiem jest kalcyt – związek o wzorze sumarycznym . | Skały gipsowe to skały, których głównym składnikiem są anhydryt () oraz gips krystaliczny – związek o wzorze sumarycznym . |
W wyniku intensywnego prażenia tego związku powstaje wapno palone, czyli oraz . | W wyniku intensywnego prażenia tego związku powstaje gips palony, czyli oraz . |
Wapno palone jest stosowane do produkcji wapna gaszonego, które jest składnikiem zaprawy murarskiej i tynkarskiej. | Gips palony i woda są składnikami zaprawy gipsowej. |
Twardnienie ww. zapraw zachodzi pod wpływem tlenku węgla(IV), dlatego zaprawę tę nazywa się powietrzną: . | Twardnienie ww. zaprawy zachodzi pod wpływem wody, dlatego zaprawę tę nazywa się hydrauliczną: . |
Węglan wapnia reaguje z kwasami, dzięki temu może być stosowany do odkwaszania gleb. Ponadto wapienie i marmur wykorzystuje się do otrzymywania materiałów budowlanych. Kreda jest skałą, którą dodaje się do m.in. białych farb, kitu, proszków i past do zębów. Po zmieszaniu z gipsem służy do wyrobu kredy do pisania. | Gips palony ze względu na łatwość wiązania wody może być stosowany np. do wytwarzania sztukaterii gipsowej, form do odlewów. Pewne ilości gipsu używa się do produkcji farb i lakierów. Szczególne zastosowanie znajduje w medycynie. Ponadto znaczne jego ilości są wykorzystywane do tworzenia wyrobów artystycznych. W rzeźbiarstwie bardzo cenionym materiałem jest alabaster. |
4. Cement, beton i zaprawa murarska
Cement, beton i zaprawa murarska to ważne materiały budowlane. Cement jest produkowany w cementowniach poprzez wypalenie mieszaniny wapieni oraz gliny i zmielenie otrzymanego spieku z gipsem krystalicznym. Beton powstaje w wyniku stwardnienia mieszaniny złożonej z cementu, kruszywa (piasku, żwiru, żużla) oraz wody w odpowiednich proporcjach, w specjalnych urządzeniach zwanych betoniarkami. Zaprawa murarska to mieszanina cementu, piasku i wody (zaprawa cementowa), często z dodatkiem wapna hydratyzowanego (zaprawa cementowo‑wapienna).

5. Hydraty i zaprawa gipsowa
Hydraty (wodziany) to uwodnione sole. Są to związki chemiczne, które zawierają cząsteczki wody wbudowane w sieć krystaliczną. Często ta sama substancja może tworzyć kilka różnych hydratów, np.: gips krystaliczny oraz gips palony – i to właśnie ten hydrat ma największe zastosowanie.

6. Alotropia pierwiastków chemicznych
Niektóre pierwiastki chemiczne, głównie niemetale, tworzą odmiany alotropowe, które mogą różnić się budową sieci krystalicznej lub liczbą atomów w cząsteczce. Mają one odmienne właściwości fizyczne i różną aktywność chemiczną. Grafit, diament, fullereny i grafen to odmiany alotropowe węgla.
Film dostępny pod adresem https://zpe.gov.pl/a/Dp7pt49kb
Alotropia węgla
7. Mydła i detergenty
Mydła i detergenty są wykorzystywane do mycia i prania, ponieważ wykazują zdolność usuwania brudu. Zbudowane są z części hydrofilowej (polarnej) oraz hydrofobowej (niepolarnej), a ich działanie polega na obniżaniu napięcia powierzchniowego wody. Mydła są wrażliwe na twardą wodę, a detergenty – nie.

8. Środki czyszczące
Obecnie do mycia i czyszczenia używa się wielu różnych preparatów. Ich starannie dobrany skład ma gwarantować skuteczność działania. Niektóre z nich mają właściwości żrące bądź drażniące, dlatego podczas ich stosowania należy zachować zalecane środki ostrożności. Nawet małe stężenia składników środków czyszczących w zbiornikach wodnych mogą przyczyniać się do degradacji środowiska przyrodniczego, dlatego chemicy stworzyli środki biodegradowalne.

9. Emulsje
Emulsja to mieszanina co najmniej dwóch niemieszających się cieczy z emulgatorem. Dodatek emulgatora utrwala emulsję. Woda jest zazwyczaj jedną fazą tego układu, natomiast drugą stanowi ciecz niemieszająca się z wodą, nazywana fazą olejową.

10. Leki
Dzięki rozwojowi medycyny i farmacji możemy w przypadku problemów ze zdrowiem stosować substancje o działaniu terapeutycznym – leki. Należy jednak pamiętać, że wszystkie leki przeznaczone dla osób chorych mogą być trucizną dla ludzi zdrowych. Ich zażywanie bez istotnej potrzeby bądź w nadmiarze może doprowadzić do przewlekłych zatruć, uszkodzenia nerek, wątroby czy szpiku kostnego. Dlatego zażywając leki, należy przestrzegać ściśle zaleceń lekarza lub farmaceuty oraz informacji podanych w ulotkach.

11. Chemiczne regulatory nastroju
Alkohol, nikotyna oraz narkotyki to kolejna grupa substancji, których spożywanie może prowadzić do uzależnienia. Alkaloidy zawarte w tych używkach działają na korę mózgową i ośrodkowy układ nerwowy.

12. Napoje
Woda jest niezbędnym elementem codziennego pożywienia i podstawowym składnikiem naszego organizmu. Aby uzupełnić ilość płynów, możemy sięgnąć nie tylko po wodę mineralną. Na półkach sklepowych można zobaczyć: soki i napoje owocowe oraz warzywne, mleko i napoje mleczne, napoje energetyczne, napoje typu cola i inne. Osoby uprawiające sport korzystają z tzw. napojów izotonicznych. Popularnymi składnikami codziennego menu są kawa i herbata, ale nie można traktować ich jako źródła wody, ponieważ działają moczopędnie.
Film dostępny pod adresem https://zpe.gov.pl/a/Dp7pt49kb
Charakterystyka różnych rodzajów napoi
13. Przetwarzanie żywności – fermentacja
Proces fermentacji, obok suszenia, jest najstarszą i najtańszą metodą utrwalania żywności. Zachodzi z udziałem mikroorganizmów (bakterii i drożdży) i może mieć przebieg beztlenowy lub tlenowy.
FERMENTACJA | ||
BEZTLENOWA | TLENOWA | |
Zastosowanie: produkcja wina, piwa i innych napoi alkoholowych, pieczenie ciasta drożdżowegopieczenie ciasta drożdżowego | Zastosowanie: wytwarzanie przetworów mlecznych, np. kefiru, jogurtówjogurtów, serów, produkcja wędlin, np. salami | Zastosowanie: wytwarzanie kwasu octowegokwasu octowego |
14. Konserwowanie żywności
Na co dzień mamy do czynienia z problemem psucia się żywności, dlatego ludzie od tysięcy lat stosowali różne metody przedłużania trwałości produktów spożywczych, m.in. poprzez dodawanie substancji konserwujących, takich jak sól kuchenna, ocet, cukier. Współcześnie obok tradycyjnych metod stosowane są nowoczesne technologie, dzięki którym uniemożliwia się lub ogranicza rozwój bakterii, drożdży i pleśni oraz zapobiega się reakcjom podstawowych składników żywności z tlenem i z wodą.

15. Zdrowa dieta
Wybór produktów, jakie codziennie spożywamy, ma ogromne znaczenie dla zapewnienia zdrowia i prawidłowego funkcjonowania naszego organizmu.
Zasady zdrowego żywienia | |
Odżywiaj się regularnie (spożywaj 4–5 posiłków dziennieposiłków dziennie) i dbaj o różnorodność tego, co jesz. | Dostarczysz organizmowi wszystkich potrzebnych substancji odżywczych oraz unikniesz nieprzyjemnych ataków odczuwania głodu. |
Spożywaj dużo warzyw i owocówwarzyw i owoców. | Zapewnisz organizmowi witaminy i składniki mineralne. Spożywaj je kilka razy dziennie także ze względu na dużą zawartość błonnika i małą zawartość tłuszczu. |
Spożywaj zdrowe węglowodany i nasionanasiona roślin strączkowych. | Dostarczysz organizmowi potrzebnych węglowodanów w produktach o niskim indeksie glikemicznym. |
Pij wodęwodę, zwłaszcza średnio zmineralizowaną. Wodę najlepiej pić małymi łykami. | W najlepszy możliwy sposób nawodnisz swój organizm. |
Unikaj nadmiaru soli i sacharozynadmiaru soli i sacharozy, zbyt dużych ilości tłuszczu, sięgaj częściej po tłuszcze roślinne niż zwierzęce. Nie pal papierosów, nie spożywaj alkoholu, nie sięgaj po narkotyki i dopalacze! | Unikniesz wielu schorzeń takich jak: otyłość, cukrzyca, próchnica zębów, osteoporoza, choroby serca, udary mózgu itd. |
Zadania
Pamiętam i rozumiem
Wymień podstawowe surowce mineralne, które służą do wytwarzania materiałów budowlanych.
Przedstaw różnice pomiędzy betonem, cementem a zaprawą budowlaną.
Omów zastosowanie każdej z odmian alotropowych węgla, nawiązując do ich właściwości.
Wytłumacz, jakie są przyczyny powstawania kamienia kotłowego w czajniku.
Wyjaśnij określenie „chleb na zakwasie”.
Opisz, jak działa lek na nadkwasotę.
Czytam i interpretuję
W dowolnym źródle (podręczniki, książki, encyklopedie, Internet) znajdź informacje, na jakiej zasadzie działają szkła fotochromowe. Wyjaśnij, dlaczego okulary fotochromowe nie spełniają dobrze swojej funkcji podczas prowadzenia samochodu, mocniej przyciemniają się w górach i poza miastem oraz nie sprawdzają się jako szkła przeciwsłoneczne latem.
Z układu okresowego odczytaj dostępne informacje na temat pierwiastków o liczbach atomowych: 6 oraz 14. Informacje te zestaw w tabeli, dopisując właściwości fizyczne i chemiczne tych pierwiastków.
Na podstawie informacji zawartych w ulotce dowolnego leku określ: w jakich przypadkach ten lek może być stosowany, w jakich dawkach, przed posiłkiem czy po nim oraz czy są jakieś szczególne wskazania związane z wiekiem osoby zażywającej lek.
Wyszukaj co najmniej trzy etykiety jogurtów i wybierz wśród nich produkt niezawierający syntetycznych dodatków do żywności oraz produkt o najdłuższym okresie przydatności do spożycia. Czy istnieje jakiś związek pomiędzy tymi danymi?
Rozwiązuję problemy
Wyjaśnij, dlaczego lampy kwarcowe są używane m.in. do dezynfekcji sal szpitalnych.
Zaprojektuj doświadczenie, aby wykazać obecność wody w chlorku kobaltu(II) – woda (1/6).
Zastanów się, jakie wiadomości poznane na lekcjach chemii przydają się podczas przygotowywania i przechowywania żywności w kuchni.
Oceń, dlaczego żyletka, liście czy owady utrzymują się na powierzchni wody, natomiast jeśli do wody dodamy płyn do kąpieli, to obiekty te toną. Jakie inne środki mogą spowodować taki sam efekt jak płyn do kąpieli?
Jaki napój warto polecić – kawę czy herbatę? Uzasadnij odpowiedź, biorąc pod uwagę właściwości składników tych napojów.
Wyjaśnij, dlaczego palenie papierosów jest szkodliwe dla zdrowia. Podaj przykłady substancji wchodzących w skład dymu papierosowego i scharakteryzuj kilka z nich.
Jakich argumentów naukowych użyjesz w dyskusji o szkodliwości nadużywania alkoholu?
Projekt badawczy
Autor/ Nauczyciel | Tytuł projektu | Badanie wpływu emulgatora na trwałość emulsji |
Temat projektu | ||
Badana hipoteza | 1. Ilość emulgatora znacząco wpływa na trwałość emulsji | |
Materiały źródłowe | Strony internetowe, działy: I, II, III w e‑podręczniku | |
Uczeń | Co dokładnie mam zamiar zrobić, by sprawdzić, czy hipoteza jest prawdziwa? | Wybrać emulsje do badań i emulgatory |
Zaplanować eksperyment: | ||
Przygotować opis wykonania eksperymentów | ||
Przygotować arkusze obserwacji eksperymentów | ||
Przeprowadzić badania | ||
Co trzeba przygotować, by zweryfikować hipotezę? | Substancje: składniki emulsji, emulgatory; sprzęt laboratoryjny: probówki, cylindry miarowe, pipety, stoper | |
Co będę obserwować (mierzyć)? | ||
Czas trwania (ile czasu potrzeba, by wykonać projekt) | 3 tygodnie na cały projekt | |
Wyniki (tabela, wykres, rysunek, fot.) | ||
Wniosek | ||
Refleksja (czego projekt mnie nauczył?) |
Zadania i polecenia dla chętnych
Wybierz stwierdzenie A lub B oraz zależność 1 albo 2 tak, aby poniższe stwierdzenie było prawdziwe.
A. | to tlenek kwasowy, ponieważ | 1. | reaguje z wodą, dając kwas | |
B. | 2. | reaguje z zasadami |
- A2
- A1
- B1
- B2
Uzupełnij tabelę.
Wzór sumaryczny | Nazwa systematyczna lub zwyczajowa | Masa cząsteczkowa | Zawartość % wody |
gorzka sól | |||
286 u | 62,94 |
Oceń prawdziwość podanych informacji.
| Prawda | Fałsz | |
| Zaprawa gipsowa jest odporna na wilgoć. | □ | □ |
| Zaprawa cementowa to materiał, który powstaje przez zmieszanie cementu, piasku i wody. | □ | □ |
| Zaprawa cementowo-wapienna jest bardziej porowata niż zaprawa cementowa. | □ | □ |
Napisz równania reakcji według schematu:
Test sprawdzający z działów: I. Materiały i tworzywa pochodzenia naturalnego, II. Chemia środków czystości, III. Chemia wspomaga nasze zdrowie. Chemia w kuchni
Test sprawdzający
Klucz testu









